近日,圣湘生物自主研發的猴痘病毒核酸檢測試劑盒(PCR-熒光探針法)通過國家藥品監督管理局審核,獲批上市。這是圣湘生物今年獲得的第十個三類醫療器械注冊證,也是圣湘新發傳染病Disease X解決方案斬獲的第一個證。

該試劑采用實時熒光PCR技術,可定性檢測人皮膚病變拭子中的猴痘病毒特異性保守區域基因,靈敏度為200copies/mL,精準性高,可及性強,可兼容多種熒光PCR平臺,搭配自動化核酸提取設備,最快60min出結果,同時采用UNG酶+dUTP防污染體系,內標監控檢測全程,保障檢測結果的準確性。
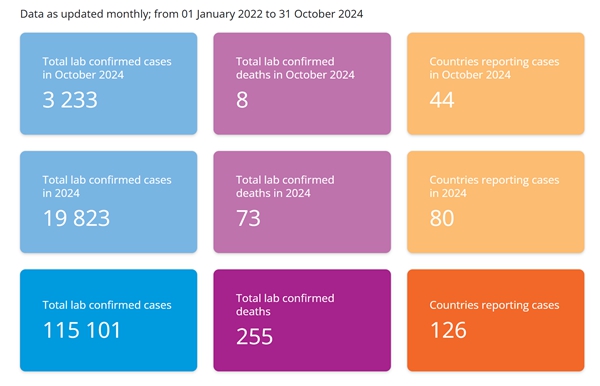
2022-2024年猴痘疫情全球趨勢
2024年8月14日,世界衛生組織(WHO)宣布猴痘疫情為國際關注的突發公共衛生事件,截至10月31日,全球126個國家/地區累計報告猴痘確診病例115,101例;同年11月22日,WHO決定維持對猴痘疫情的最高級別警戒,理由是病例和受影響國家的數量在繼續上升。
作為一種典型的病毒性人畜共患病(從動物傳播給人的病毒),猴痘病毒(Monkeypox virus, MPV)主要發生在非洲中部和西部地區熱帶雨林,感染后的主要癥狀包括發熱、淋巴結腫大和全身水皰膿皰,與一些出疹性疾病(如水痘、天花、單純皰疹等)存在相似之處,僅靠臨床癥狀對病原進行區分并不可靠。
目前實驗室檢測猴痘病毒的主要方法包括:病毒分離和鑒定、血清學檢測、PCR檢測、抗原抗體檢測等。WHO在8月29日發布的猴痘EUL邀請中指出產品定位在分子產品,血液和抗體檢測不推薦用于常規診斷;WHO發布的《全球猴痘戰略準備與應對計劃》明確指出,PCR檢測是針對猴痘病毒診斷的金標準,可以快速、準確地區分猴痘病毒與其他相似病毒,對于疾病的早期診斷和疫情防控非常重要。
近年來,圣湘生物針對猴痘病毒開發了一系列檢測產品,可滿足各類檢測場景需求。其中,猴痘病毒核酸檢測試劑在今年8月份成為非洲疾病預防控制中心(Africa CDC)首批推薦檢測試劑;2022年到2024年期間,作為FIND基金會推薦使用參考試劑,用于評估其他猴痘檢測試劑的準確性。目前,該試劑已經取得歐盟、英國、北愛爾蘭、哥倫比亞、印度尼西亞、沙特、摩洛哥等多個地區和國家的注冊準入證書,并出口至法國、菲律賓、馬來西亞、土耳其、印度尼西亞等20多個國家,助力全球猴痘疫情防控。

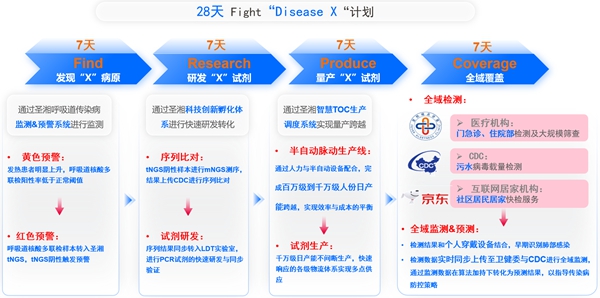
圣湘生物此次上市的猴痘病毒核酸檢測試劑是圣湘已搭建的新發傳染病“Disease X”解決方案的第一證。該方案集儀器、試劑、數智化系統為一體,通過強大的研發生產體系實現7天發現“X”病原,7天研發“X”試劑,7天量產“X試劑”,7天全域覆蓋,在28天完成對人源樣本和環境污水等樣本的“檢測—監測—預測”全流程管理,有效提高對Disease X的防控能力,在疾病出現早期及時發現、準確監測,并對其發展趨勢進行科學預測,從而為制定合理的防控策略和保障全球公共衛生安全提供有力支持。

